|
碳纳米管修饰电极电催化还原去除废水中的氯霉素氯霉素具有良好的抗菌作用和药物代谢动力学特性,在控制和治疗家畜、 家禽、 蜜蜂和水生动物的传染性疾病中发挥了重要作用[1, 2]. 但是,氯霉素能够抑制人体骨髓造血功能,引起再生障碍性贫血,甚至诱发癌症[3]. 为此,美国、 欧盟等国家和组织将氯霉素列为违禁药物,规定不得在动物源性食品中检出,我国也于2002年规定在动物疫病防治中禁止使用氯霉素. 由于氯霉素的广谱抗菌作用,使用方便且价格低廉,被非法使用的现象时有发生[4]. 氯霉素可以通过动物排泄、 污废水排放和降雨径流等途径进入水环境,并持续污染水体,在海水[5]、 城市污水[6, 7]、 养猪场废水[8]和污水处理厂出水[9, 10]中均能检出氯霉素的存在. 水环境中的氯霉素不仅能使细菌产生抗性基因,还可通过食物链进入人体,严重威胁生态环境安全和人体健康. 因此,发展废水中氯霉素的有效去除方法显得极其重要. 目前,废水中氯霉素的去除方法主要有传统处理法(聚沉、 絮凝和微生物降解等)[11]、 吸附法[12]、 臭氧氧化法[13]、 辐射与光分解法[14, 15]、 Fenton氧化法[16]等,但是,这些方法存在处理效率低、 投资大、 能耗高或容易造成二次污染等问题. 电化学法包括电氧化法和电还原法,具有高效、 低成本、 操作简便和环境友好等特点,电氧化法已用于酚类化合物和染料废水的处理研究[17]. 但是,电氧化处理有机物通常需要较高的氧化电位,氧化电位过高不仅增加能耗,严重腐蚀电极,还会加剧析氧、 析氯等副反应. 近年来,电还原处理抗生素显现出一定的潜力,孙飞等[18]和Liang等[19]用非生物阴极还原氯霉素,处理24 h时的去除率分别达到57.9%与73.0%,但是这些方法的处理能力受到电极材料的制约. 碳纳米管具有长径比和比表面积大、 稳定性强和量子效应明显等特性,用做修饰材料可以降低电极的过电势,增加电流响应,提高电极的选择性和灵敏度,现在主要用于氯霉素的测定研究[20, 21],鲜见用于去除废水中氯霉素的报道. 由于缺乏有效的试剂分散碳纳米管,通常将碳纳米管直接超声分散在纯水中,造成成膜效果不理想,影响修饰电极的电催化活性. 表面活性剂同时具有亲水和疏水性质,能够将碳纳米管有效地分散在水中[22]. 为此,本研究在筛选表面活性剂的基础上,优化碳纳米管与表面活性剂的配比、 分散液修饰量,制备碳纳米管修饰电极,分析修饰电极对模拟废水中氯霉素的去除能力,初步探讨氯霉素的还原去除机制,以期为发展废水中抗生素的处理技术、 保护水环境质量提供科学依据. 1 材料与方法 1.1 主要试剂 氯霉素标准品(分析纯,纯度 ≥ 98.5%)购自德国Dr. Ehrenstorfer公司; 乙腈和甲醇均为色谱纯,购自Fisher Scientific公司; 双十六烷基磷酸(DHP)购自上海将来生化试剂公司,十二烷基硫酸钠(SDS)和十六烷基三甲基溴化铵(CTAB)均购自成都科龙化学试剂公司; 其余试剂均为分析纯,购自成都科龙化学试剂公司. 羧基化多壁碳纳米管(MWCNTs): 纯度>95%,管径为8~15 nm,长度为0.5~2 μm,南京先丰纳米材料科技有限公司生产. 含氯霉素的模拟废水: 准确称取1 g氯霉素(纯度为96%,合肥博美生物科技有限公司),加入100 mL甲醇溶解,用去离子水稀释至1000 mL,配制成质量浓度为1000 mg·L-1的贮备溶液,于4℃避光保存. 临用前根据需要,取氯霉素贮备液,用不同电解质溶液(0.1 mol·L-1 HAc-NaAc、 Na2SO4、 NH3·H2O-NH4Cl、 Na2HPO4-NaH2PO4溶液)稀释,配制成质量浓度为1、 2、 5、 10 mg·L-1的氯霉素工作溶液. 1.2 主要仪器 电化学工作站: CHI 660E型,上海辰华仪器有限公司,工作电极为碳纳米管修饰的玻碳电极(直径3 mm),对电极为铂丝电极(直径1 mm),参比电极为饱和甘汞电极(SCE); 扫描电子显微镜(SEM): JSM-7800F型,日本电子株式会社; 激光粒度与Zeta电位分析仪: ZetaPlus型,美国Brookhaven仪器公司; 高效液相色谱分析仪: LC-20A型,配SPD-20A紫外检测器,日本Shimadazu公司; 液相色谱-串联质谱分析仪: API 4000型,美国AB SCIEX公司. 1.3 实验步骤与方法1.3.1 碳纳米管修饰电极的制备 电极的预处理: 在麂皮上用Al2O3粉末(粒径为0.3 μm)将玻碳电极(GCE)表面抛光成镜面,依次用超纯水、 无水乙醇和超纯水超声清洗,每次清洗5 min. 碳纳米管的分散: 取适量MWCNTs粉末和表面活性剂,加入超纯水,超声分散20 min,获得均匀的碳纳米管分散液(1 mg·mL-1),4℃密封保存备用. 修饰电极的制备: 取适量碳纳米管分散液,均匀滴涂到处理好的GCE表面,室温下风干待用. 1.3.2 模拟废水中氯霉素的电催化还原 分别移取5 mL质量浓度为1、 2、 5、 10 mg·L-1的氯霉素溶液于电解池(直径约1.5 cm、 高约4 cm)中,锡箔纸覆盖后置于磁力搅拌器上,室温恒速搅拌,浸入碳纳米管修饰电极、 铂丝电极和饱和甘汞电极,在时间-电流法模式下电催化还原氯霉素. 取还原12 h的反应液1 mL,过0.22 μm有机滤膜,用高效液相色谱法(HPLC)测定氯霉素含量,计算氯霉素的去除率. 每个实验重复3次,下同. 实验结束,取出碳纳米管修饰电极,置于0.1 mol·L-1 NH3·H2O-NH4Cl溶液,在偏压为1.5 V下去钝化30 min,对电极进行再生. 1.3.3 表面活性剂的筛选和电极修饰条件优化 取DHP、 SDS和CTAB等3种表面活性剂,分别与MWCNTs混合,加入超纯水并超声分散20 min,于4℃下静置,观察MWCNTs在超纯水中的稳定情况; 取MWCNTs分散液1 mL,测定Zeta电位,筛选出辅助分散效果最好的表面活性剂. 按照1.3.1节的步骤,以MWCNTs与表面活性剂的配比分别为1∶2、 1∶1和2∶1,分散液修饰量分别为5、 10、 15、 20和25 μL,制备碳纳米管修饰电极,考察修饰电极电催化还原2 mg·L-1氯霉素的效果. 1.3.4 电催化还原条件的优化 按照1.3.2节的实验步骤,考察偏压、 底液、 初始pH对2 mg·L-1氯霉素去除率的影响,其中偏压为-0.6、 -0.7、 -0.8、 -0.9、 -1.0、 -1.1和-1.2 V,底液为0.1 mol·L-1 HAc-NaAc、 Na2SO4、 NH3·H2O-NH4Cl和Na2HPO4-NaH2PO4溶液,初始pH为4、 5、 6、 7、 8、 9和10. 1.3.5 电催化还原氯霉素的动力学特征 移取5 mL质量浓度为2 mg·L-1的氯霉素溶液于电解池中,用锡箔纸覆盖避光,置于磁力搅拌器,室温恒速搅拌,在最优实验条件下分别还原2、 4、 6、 8、 10、 12、 14、 16、 18、 20、 22和24 h,取反应液1 mL,过0.22 μm有机滤膜,测定滤液中氯霉素含量,研究电催化还原氯霉素的动力学特征. 1.3.6 氯霉素及其还原产物的测定与质量控制 采用HPLC分离、 紫外检测器测定氯霉素的含量[23]. 色谱柱: Inertsil ODS-SP色谱柱(250 mm×4.6 mm; 5 μm),柱温为30℃; 流动相为20%乙腈-水溶液,流速为0.8 mL·min-1,等度洗脱; 进样量为20 μL. 通过紫外全波长扫描,确定检测波长为274 nm. 外标法定量,获得氯霉素的检出限为9.6 μg·L-1,在7个加标水平的回收率为80.15%~106.8%,相对标准偏差(RSD)为5.17%~9.86%. 采用液相色谱-串联质谱法(LC-MS/MS)鉴定氯霉素的还原产物. 色谱条件: Acquity UPLC BEH C18色谱柱(100 mm×2.1 mm,1.7 μm,Waters),柱温为40℃; 流动相为55%甲醇-水溶液,流速为0.3 mL·min-1; 进样量为5 μL. 质谱条件: 碰撞气为氩气,锥孔气和雾化气均为高纯氮气; 负离子化模式,喷雾电压为4500 V,温度为550℃; 全扫描模式监测. 2 结果与讨论2.1 碳纳米管修饰电极的制备条件2.1.1 表面活性剂的筛选 考察了在SDS、 CTAB和DHP等3种表面活性剂作用下,碳纳米管在超纯水中的分散效果. 在SDS和CTAB作用下,MWCNTs分散液分别放置27 d和45 d基本沉降完全; 在DHP作用下,MWCNTs分散液放置3个月未发现沉降现象. 结果表明,DHP是碳纳米管的一种有效助散剂,使得碳纳米管在纯水中分散均匀、 性质稳定. 从分子结构上来看,SDS分子中含有一条12个碳原子的疏水长链,CTAB分子中含有一条16个碳原子的疏水长链,而DHP分子中含有两条16个碳原子的疏水长链,使得3种表面活性剂的疏水性表现为DHP>CTAB>SDS,在超声时DHP能够促使碳纳米管被均匀分散到纯水中,形成更加稳定的悬浮液[20]. Zeta电位分析发现,SDS、 CTAB和DHP辅助分散的碳纳米管悬浮液的Zeta电位分别为-28.10、 -31.26和-40.18 mV. Zeta电位的绝对值越大,胶体粒子表面所带的同种电荷越多,使得胶体粒子越分散,在DHP作用下胶体粒子的稳定性最强,因此选用DHP辅助分散碳纳米管. 2.1.2 MWCNTs和DHP的配比 考察了MWCNTs和DHP的配比对修饰电极电催化还原氯霉素的影响. 当MWCNTs和DHP的配比为1∶2、 1∶1和2∶1时,电催化还原12 h时氯霉素的去除率分别达到72.96%、 82.25%和75.83%,说明MWCNTs和DHP的配比为1∶1时氯霉素的去除率最高. 分散液中MWCNTs和DHP的配比过低或过高都不利于氯霉素的还原,这是因为DHP本身不导电[21],当DHP的占比高时,阻碍电子传递; 当DHP的占比低时,MWCNTs不能充分分散在超纯水中,部分MWCNTs发生沉降,使得修饰到GCE表面的碳纳米管相对较少,降低了氯霉素的还原率. 因此,确定MWCNTs和DHP的配比为1∶1. 2.1.3 分散液修饰量 考察了分散液修饰量对修饰电极电催化还原氯霉素的影响. 在电催化还原12 h时,氯霉素的去除率随电极上分散液修饰量的增加而逐渐增加; 当修饰量为15 μL时,氯霉素的去除率达到最大(82.25%); 随后去除率随修饰量的增加而逐渐减小. 这是因为随着分散液修饰量的增加,GCE表面的活性位点增加,加快了电子传递,有利于氯霉素的还原; 当修饰量超过15 μL时,会使GCE表面的碳纳米管变厚,阻碍电子在溶液与电极间传递,导致氯霉素的还原率下降. 因此,确定分散液修饰量为15 μL. 2.2 碳纳米管修饰电极的表征 图 1表示DHP和MWCNTs/DHP的扫描电镜图. 从中可以看出,未超声分散的DHP为块状和片状晶体[图 1(a)]; 超声分散的MWCNTs/DHP复合物具有明显的碳纳米管形态结构[图 1(b)],碳纳米管相互缠绕,其间夹杂着小块状的DHP晶体,与DHP单体具有显著差异.  图 1 DHP和MWCNTs/DHP的扫描电镜图 图 2为碳纳米管修饰电极和裸GCE在含有5mmol·L-1 K3[Fe(CN)6]的0.1 mol·L-1 KCl溶液中的循环伏安图. 从中可以看出,碳纳米管修饰电极的氧化峰电流(120 μA)远大于裸GCE(58 μA),还原峰电流(127 μA)也远大于裸GCE(69 μA),表明修饰碳纳米管后有利于电子在溶液和电极间传导,具有优良的电催化潜力,也证实碳纳米管被成功修饰到GCE上. 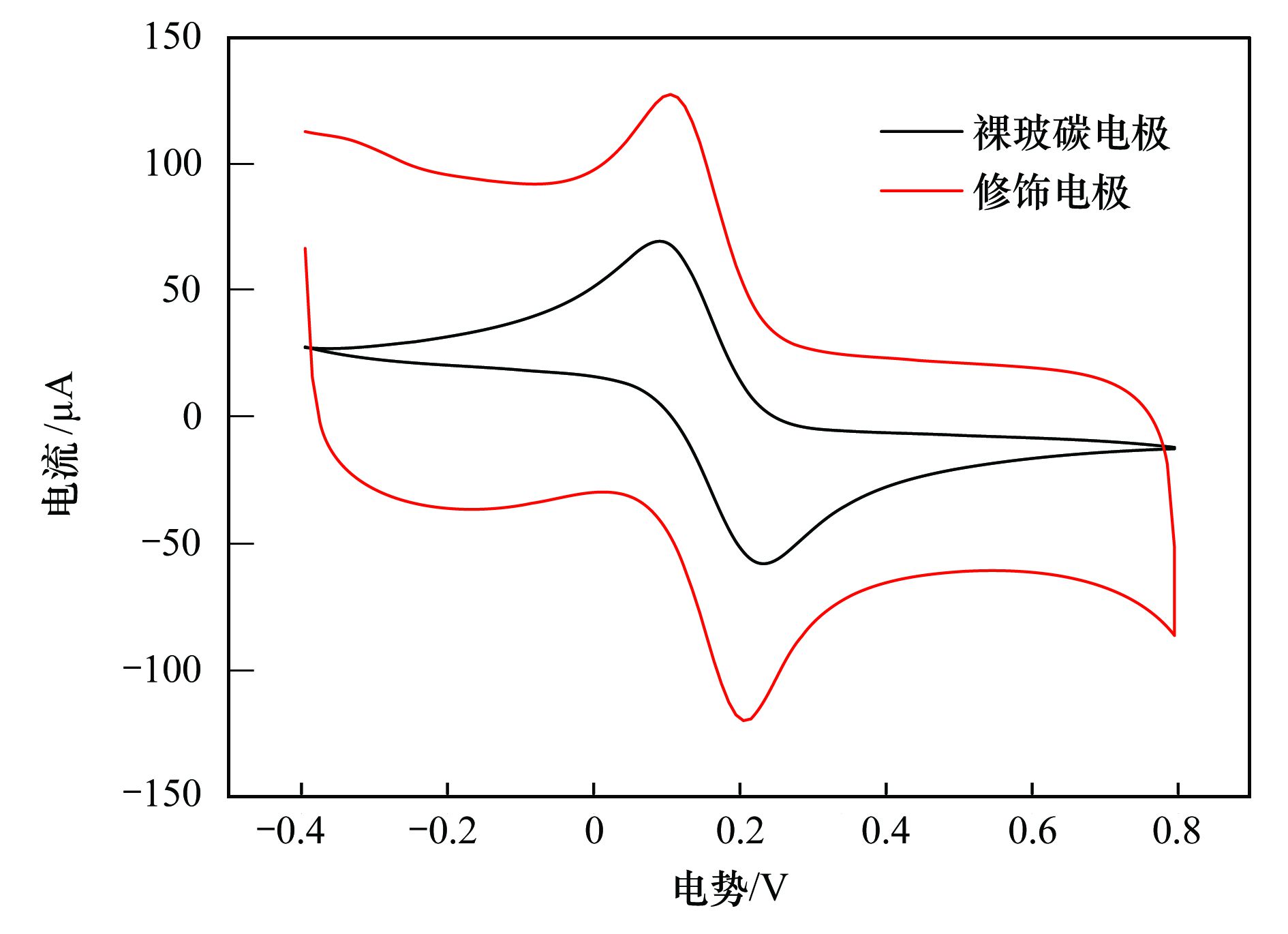 图 2 碳纳米管修饰电极和裸玻碳电极的循环伏安图 2.3 氯霉素的电催化还原条件2.3.1 偏压 利用电化学工作站输出额定偏压,研究偏压对电催化还原氯霉素的影响,获得的结果如图 3所示. 从中可以看出,随着偏压的增加,氯霉素的去除率逐渐升高,当偏压为-1.2 V时,氯霉素的去除率达到86.59%. 有研究指出,阴极电位越负,作为电子受体的污染物还原效率越高[24]. 但是,在偏压为-1.2 V时工作电极表面有大量气泡产生,其原因可能是过电势增大使得电极表面发生了析氢反应; 当偏压为-1.1 V时,工作电极表面未观察到气泡产生,氯霉素的去除率达到82.25%. 为了避免析氢反应和减少能耗,本研究确定偏压为-1.1 V. 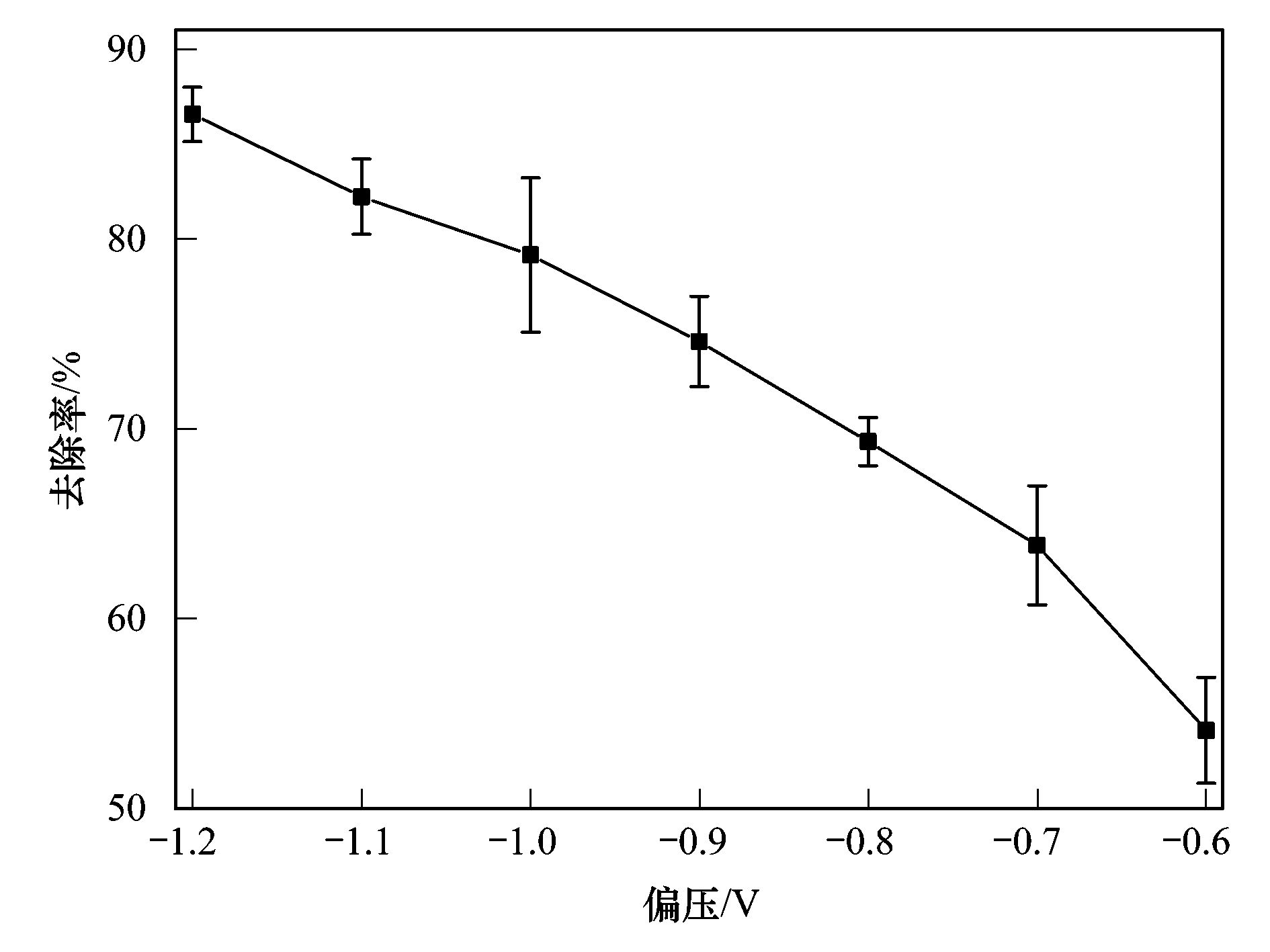 图 3 偏压对电催化还原氯霉素的影响 2.3.2 底液 在偏压为-1.1 V时,考察了底液对电催化还原氯霉素的影响. 有研究发现,在初始pH为7的0.1 mol·L-1的HAc-NaAc、 Na2SO4、 NH3·H2O-NH4Cl、 Na2HPO4-NaH2PO4溶液中,氯霉素的去除率分别为56.32%、 68.78%、 82.25%和70.13%,说明在NH3·H2O-NH4Cl溶液中更有利于氯霉素的还原. 张金磊等[25]用循环伏安法测定氯霉素时,也发现在NH3·H2O-NH4Cl溶液中氯霉素的还原峰电流最大. 因此,本研究选择NH3·H2O-NH4Cl溶液为底液. 2.3.3 底液初始pH 考察了底液初始pH对电催化还原氯霉素的影响,获得如图 4所示的结果. 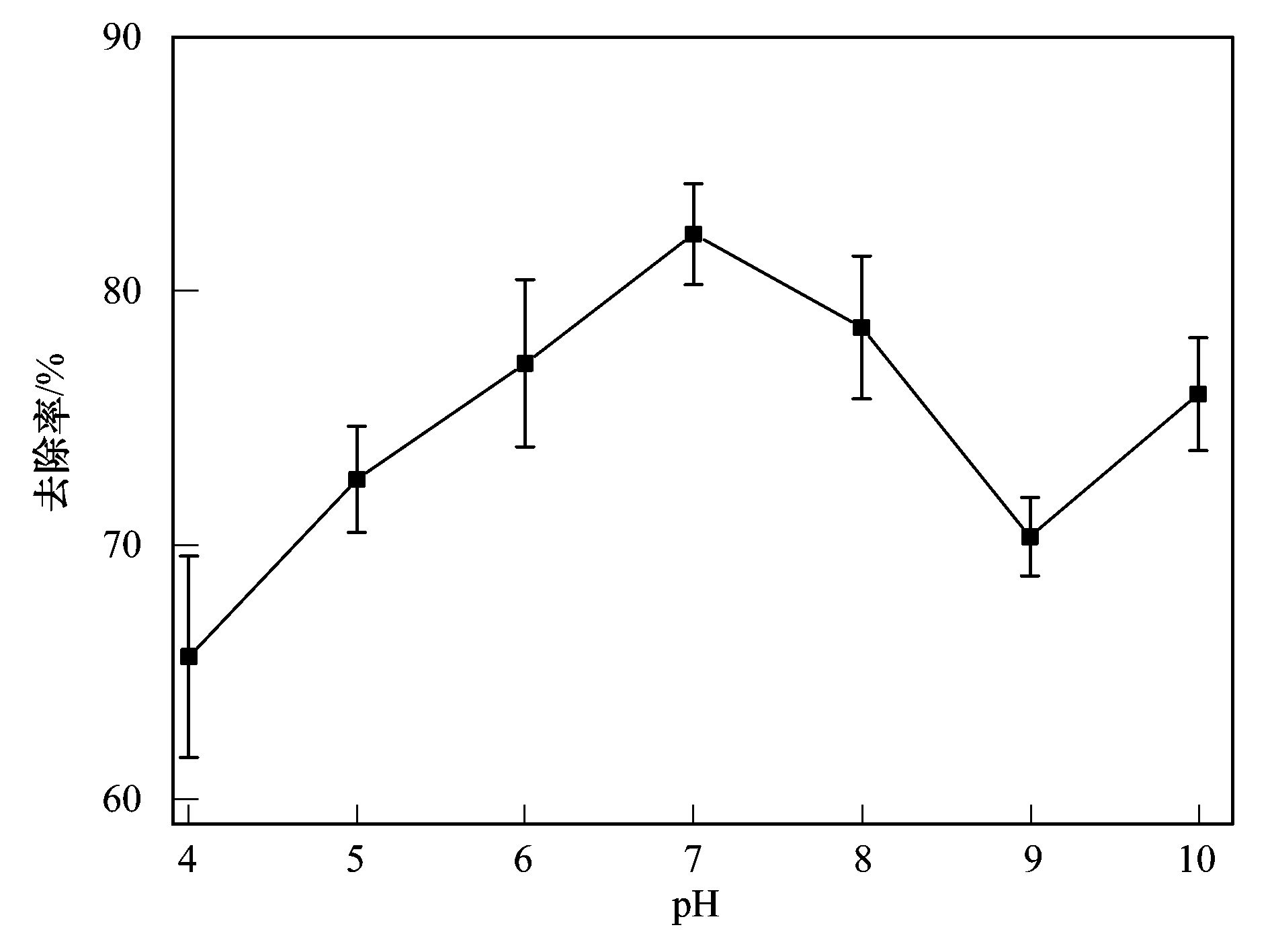 图 4 底液初始pH对电催化还原氯霉素的影响 从图 4可以看出,随着底液初始pH的增加,氯霉素的去除率逐渐增大; 在pH为7时,获得最大去除率为82.25%,随后逐渐减小; 当pH为9时,去除率下降为70.33%. 总体来看,酸性或碱性条件均不利于氯霉素的电催化还原. 在pH为10时氯霉素的去除率又开始上升,这是因为在pH>9后氯霉素容易发生水解[26],导致其还原率出现假性增大. Zhuang等[27]在用循环伏安法测定氯霉素时,也发现其还原峰电流在pH为7时达到最大,说明中性环境更有利于电子传导. 因此,本研究确定底液的初始pH为7. 在最优的实验条件下,考察了碳纳米管修饰电极对氯霉素的电催化还原能力,获得初始浓度为1、 2、 5和10 mg·L-1的氯霉素被还原12 h时的去除率分别为89.93%、 82.25%、 72.31%和67.36%,随着氯霉素浓度的增加,传质阻力相应增大,使得氯霉素的去除率下降. 该修饰电极通过去钝化处理后,还原1 mg·L-1氯霉素12 h时的去除率能够达到80%以上,说明该电极特别适合于处理低浓度氯霉素废水. 2.4 电催化还原氯霉素的动力学特征 反应液中氯霉素浓度随时间的变化如图 5所示. 从中可以看出,氯霉素浓度随时间的增加逐渐减小,在0~10 h时表现为快速还原过程,10~18 h表现为慢速还原过程,随后趋于稳定; 获得还原氯霉素24 h时的去除率为97.21%,远远高于在裸GCE上的去除率(53.69%),表明采用碳纳米管修饰电极能够显著提高氯霉素的去除率. 比较发现,本研究获得氯霉素的去除率远大于其在非生物阴极上还原24 h时的去除率(57.9%)[18]; 通过接种微生物的生物阴极还原氯霉素,24 h时氯霉素的去除率可以提高到96.0%[19],还是低于本研究的去除效果. 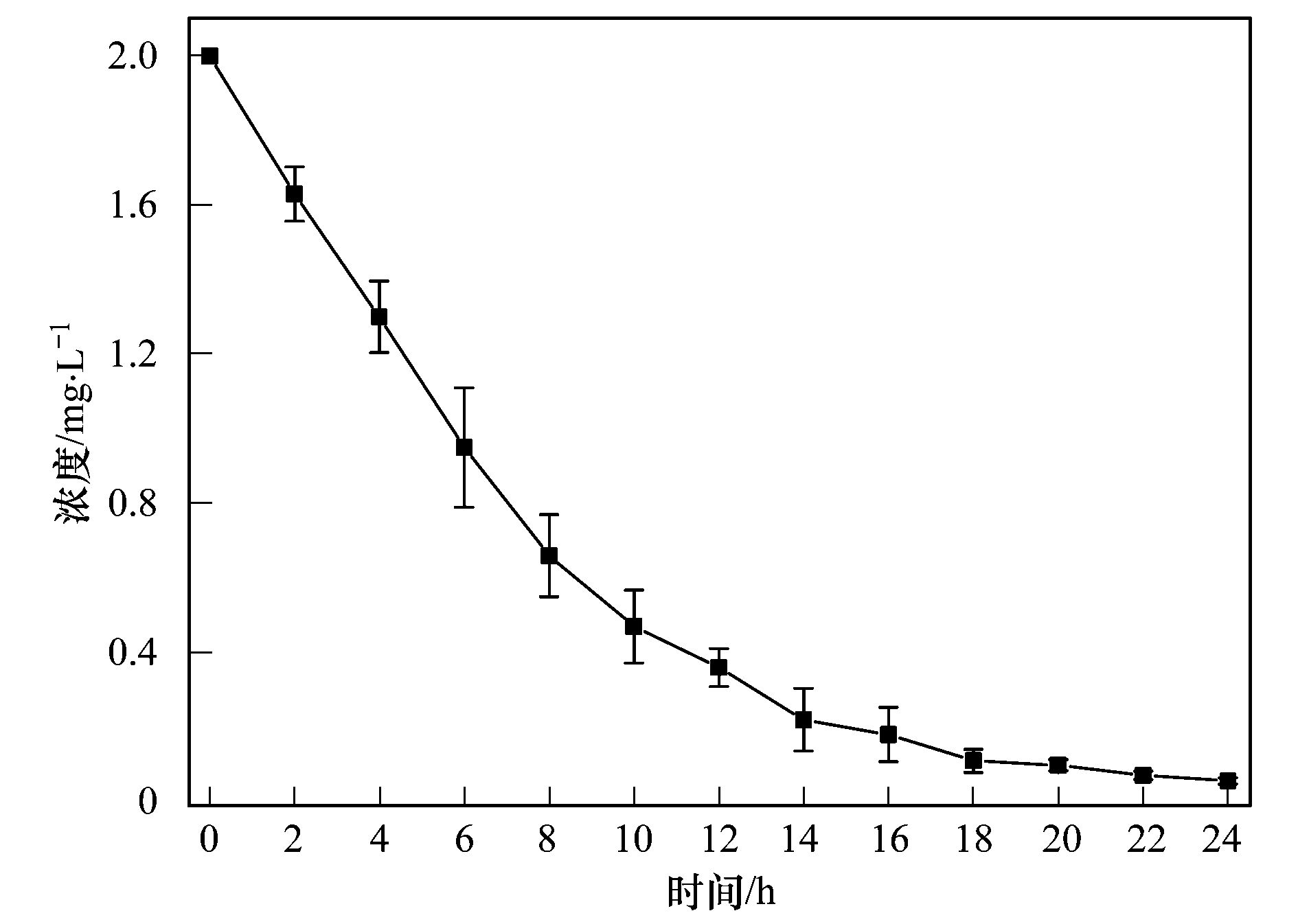 图 5 电催化还原氯霉素的动力学曲线 采用零级、 一级和二级反应动力学模型拟合实验数据,获得如表 1所示的结果. 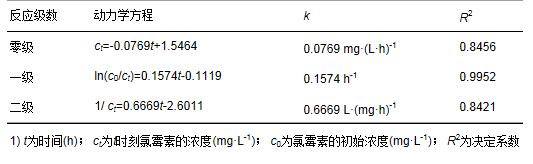 表 1电催化还原氯霉素的动力学特征1) 从表 1可以看出,采用一级反应动力学模型可以很好地描述氯霉素的电催化还原过程,获得去除速率常数为0.1574 h-1,半衰期为4.40 h. Liang等[19]用非生物阴极、 Sun等[28]用生物阴极还原氯霉素也遵循一级反应动力学方程,分别获得的非生物阴极还原的速率常数(0.052 h-1)和生物阴极还原的速率常数(0.084 h-1)均明显低于本研究,说明采用碳纳米管修饰电极能够明显加快氯霉素的还原. 2.5 电催化还原氯霉素的机制分析 取电催化还原氯霉素0和24 h的反应液,采用液相色谱-串联质谱法(LC-MS/MS)鉴定反应产物,获得如图 6所示的结果. 从图 6可以看出,还原氯霉素(CAP)0 h时,在质谱中发现峰强度最高的氯霉素特征峰(质荷比为321.1) 与生物阴极还原氯霉素的报道[4, 19, 29]吻合;还原氯霉素24 h时,出现了峰强度较低的质谱峰(质荷比为294.6) 和峰强度最高的特征峰(质荷比为261.2) ,分别被鉴定为羰基还原的AMCl2、 脱去1个氯原子的羰基还原的AMCl. 在用生物阴极还原氯霉素的产物中也得到类似结果,鉴定出羰基还原的AMCl2(48 h)和脱去2个氯原子的羰基还原的AM(144 h)[29],本研究采用碳纳米管修饰电极和更负的偏压(-1.1 V)加快了氯霉素的还原进程,随着时间的推移,羰基还原的AMCl可能会进一步脱去另1个氯原子. 在非生物阴极还原氯霉素的产物中,除发现羰基还原的AMCl2外,还鉴定出具有强抗菌活性的中间产物亚硝基和羟氨基化合物(—NO2分别被还原为—NO和—NHOH)[30],当偏压为-0.4 V时羰基还原的AMCl2难以进一步脱氯转化为羰基还原的AMCl,而在-0.7 V时容易进一步脱氯转化为羰基还原的AMCl[19],很好地解释了本研究在-1.1 V电催化还原氯霉素鉴定出羰基还原的AMCl[图 6(b)]的事实,未发现亚硝基和羟氨基化合物的原因可能是还原24 h时这些中间产物已经被完全转化. 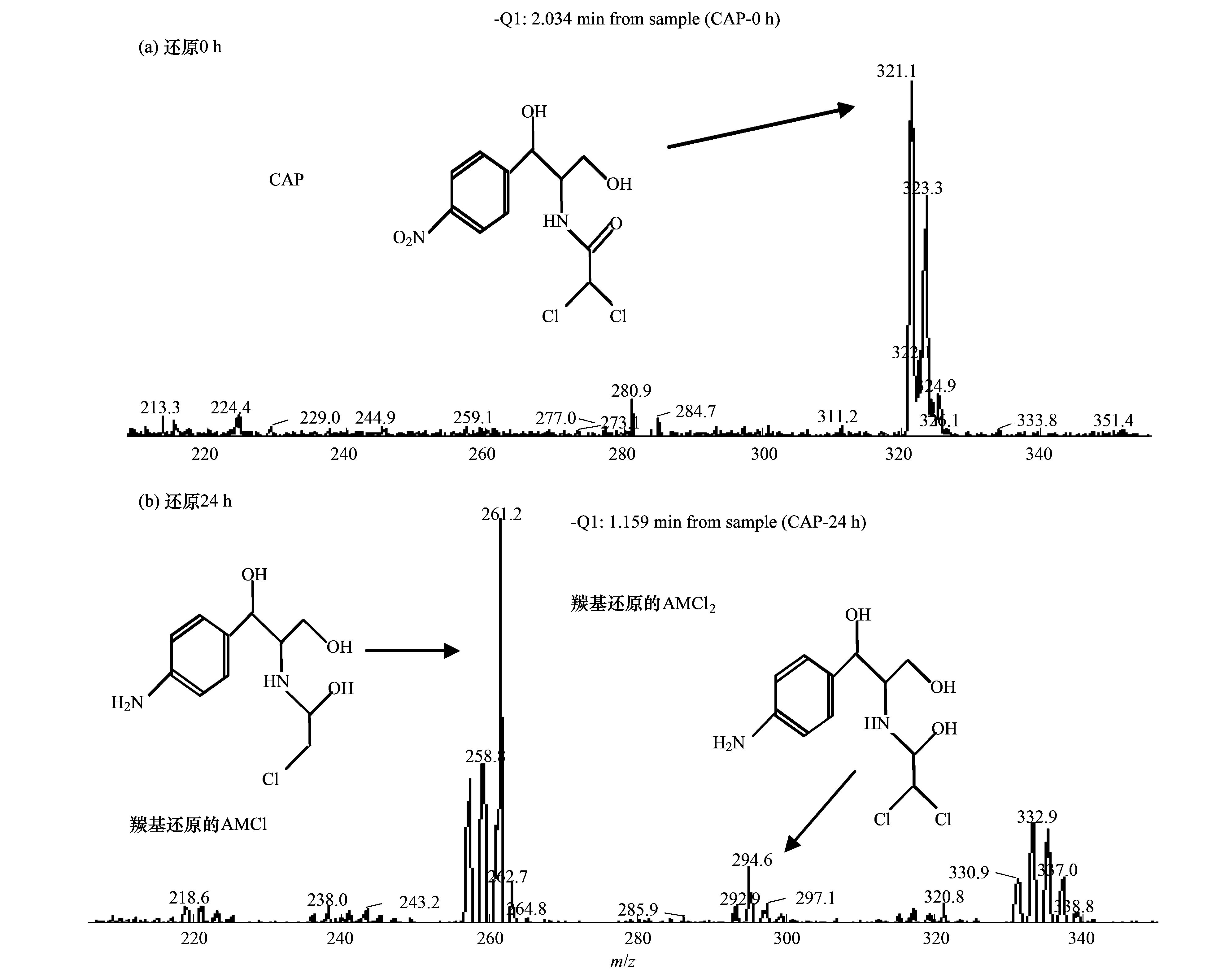 图 6 氯霉素还原产物鉴定 基于以上分析,获得电催化还原氯霉素的可能途径(见图 7). 从中可以看出,在碳纳米管修饰电极电催化还原过程中,氯霉素获得2、 4、 6、 8和10个电子,被分别转化为亚硝基化合物、 羟氨基化合物、 AMCl2、 羰基还原的AMCl2和羰基还原的AMCl,由于生成羰基还原的AMCl2和羰基还原的AMCl,不仅还原了氯霉素中决定抗菌性的硝基基团[31],还可以进一步还原羰基和脱氯,显著降低氯霉素的毒性. 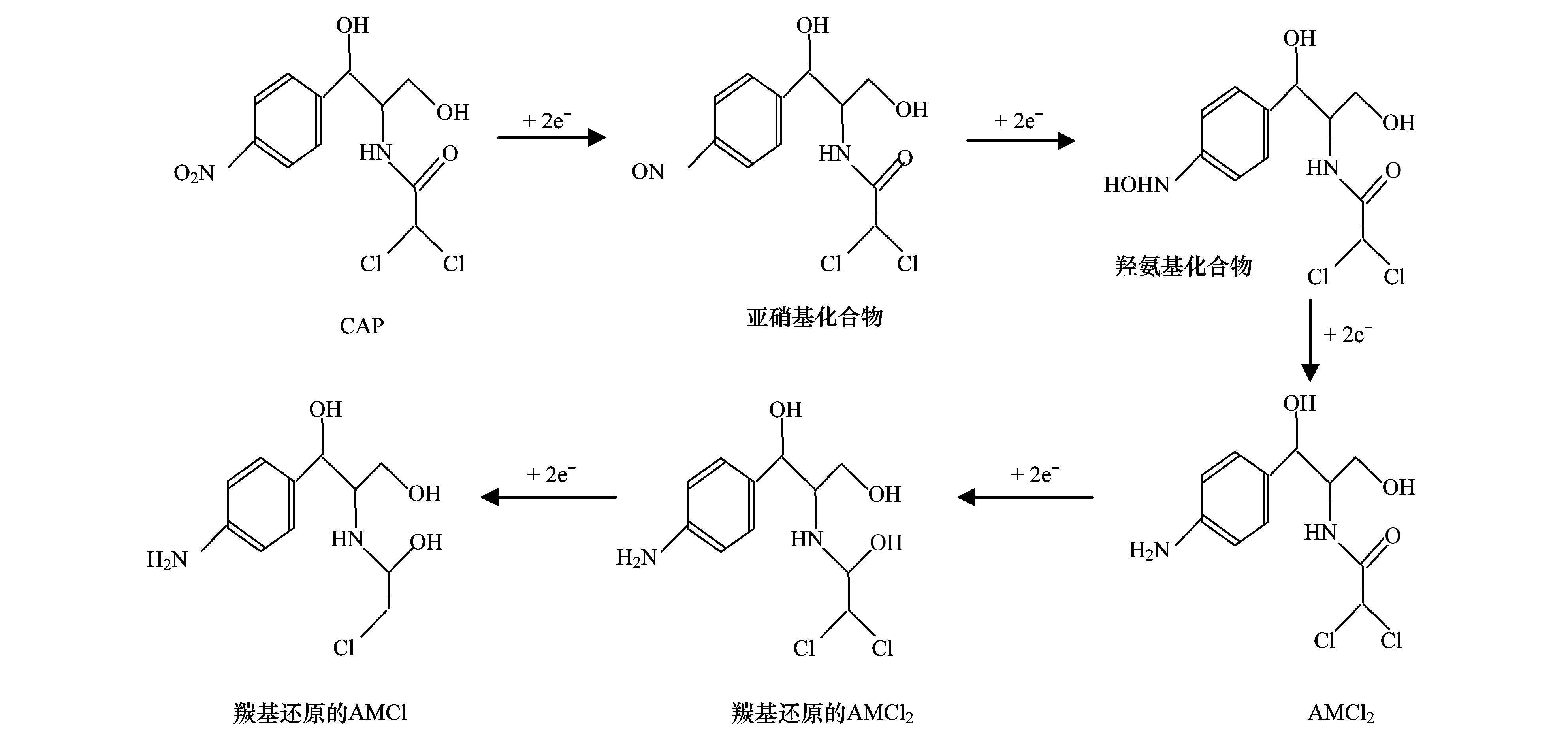 图 7 电催化还原氯霉素的可能途径 3 结论 (1) 获得了碳纳米管修饰电极的最佳制备条件,即采用DHP辅助分散碳纳米管,MWCNTs和DHP的配比为1∶1,分散液修饰量为15 μL; 获得了电催化还原氯霉素的最佳条件,即偏压为-1.1 V,底液为0.1 mol·L-1 NH3·H2O-NH4Cl溶液,初始pH为7. (2) 电催化还原氯霉素的动力学过程符合一级反应动力学模型,去除速率常数为0.1574 h-1; 氯霉素被还原24 h的去除率达到97.21%,特别适合于低浓度氯霉素废水的处理. (3) 采用碳纳米管修饰电极电催化还原氯霉素,不仅还原了氯霉素中决定抗菌性的硝基基团,还可以进一步还原羰基和脱氯,显著降低氯霉素的毒性. |

